Calcul des angles dans la molécule de méthane
Voici un petit exercice de géométrie élémentaire dans l’espace. Il est inspiré par une question sur le blog de Pierre Lecomte et la petite discussion qui lui suivait concernant les symétries d’un cube.
La molécule méthane CH4 est un tetraèdre régulier avec l’atome de carbone au centre. Déterminer, si possible avec un minimum de calcul, l’angle entre deux liaisons hydrogène-carbone.
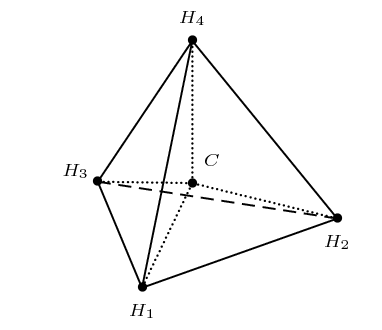
En fait il s’agit d’un exercice classique pour les chimistes. Ici je numérote les quatre atomes d’hydrogène H1, H2, H3 et H4 pour que vous puissiez les distinguer dans vos calculs.

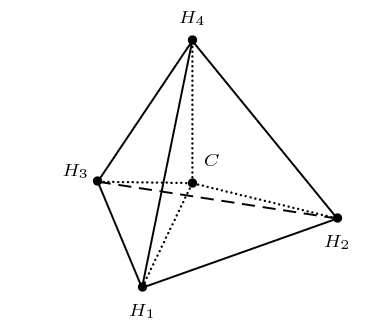

Arcos(-1/3)
J’ai trouvé une démo très élégante, mais la marge est trop petite pour la contenir.
bon j’avoue c’est assez laid comme démo, on se place dans un repère orthonormé où les H ont des coordonnées simples ((1,0,0),(0,1,0),(0,0,1),(1,1,1)), on trouve les coordonnées de C, et on fait du produit scalaire. Pas d’histoire de rotation ou autre 🙁
Je trouve la même chose mais sans géométrie analytique.
Il est facile de calculer \(l=\|CH_4\|\) en fonction de la longueur \(a\) des côtés du tétraèdre. Je trouve
\(\frac{\sqrt 3}{2\sqrt 2}a\)
Voici la démarche : la droite \(H_4C\) perce le triangle \(H_1H_2H_3\) en son centre de gravité \(G\) et lui est perpendiculaire. De plus \(l=3\|H_4G\|/4\). On calcule \(\|H_4G\|\) dans le triangle rectangle \(H_4H_1G\) (on connait la longueur des hauteurs des triangles équilatéraux et \(\|H_1G\|\) en vaut les deux tiers).
Pour calculer le cosinus de l’angle cherché, il suffit alors d’appliquer le théorème de Pythagore généralisé au triangle isocèle \(H_4CH1\).
Merci pour vos solutions. En fait, je pensais à celle proposée par Ylrahc qui utilise le choix d’un repère adapté dans lequel le calcul du produit scalaire est simple car les coordonnées des atomes sont immédiates. Pour expliquer que le centre du tétraèdre est égal au centre du cube on peut utiliser le fait que les diagonales du cube sont des axes de rotation d’ordre trois qui laissent invariant pas seulement le cube mais aussi le tétraèdre; elles coïncident donc avec les hauteurs du tétraèdre 😉
Le dessin du commentaire 4 met bien en évidence le triangle isocèle C H1H2 dont les angles égaux
valent Arctg(1/Sqrt[2]), angle d’une diagonale du cube avec sa base.
L’angle des deux liaisons vaut donc 180 – 2 Arctg (1/Sqrt[2]).
Merci pour la figure.
Oui, c’est encore plus élémentaire ! En résumé, on trouve donc que l’angle entre l’atome de carbone et deux atome d’hydrogène vaut arccos(-1/3) = 180° – 2 arctan(2-1/2). C’est environ 109,47°.
Il y a un autre choix amusant de coordonnées : on peut se placer dans R4 et prendre pour sommets du tétraèdre les points (1,0,0,0) ; (0,1,0,0) ; (0,0,1,0) et (0,0,0,1).
L’avantage est que le résultat est aussitôt généralisable en toute dimension…
Oui, ces quatre points forment un tétraèdre régulier de centre (1/4,1/4,1/4,1/4), et on obtient encore le même résultat. Merci pour cette belle idée!
Je trouve cette idée très jolie également!
Démonstration « pour chimiste »
En faisant de la chimie, je suis tombé sur l’angle de \(\alpha\)=109,47° pour une configuration tétraédrique. Et je ne voyais pas d’où cela sortait.
Je suis parti du constat que même si les liaisons sont polarisées, la molécule elle ne l’est pas. En projetant sur l’une des liaisons les dipôles électriques de toutes les liaisons on obtient +1+3*cos(\(\alpha\))=0. On en déduit \(\alpha\)=arccos(-1/3)=109,47° à 10^-2 près.
Merci pour votre commentaire. Quand vous écrivez « en projetant sur l’une des liaisons » vous utilisez bien le produit scalaire, non?